产品
iNeo–Vac 系列


IND approved

IIT
IIT
iNeo-ABassistantTM 平台
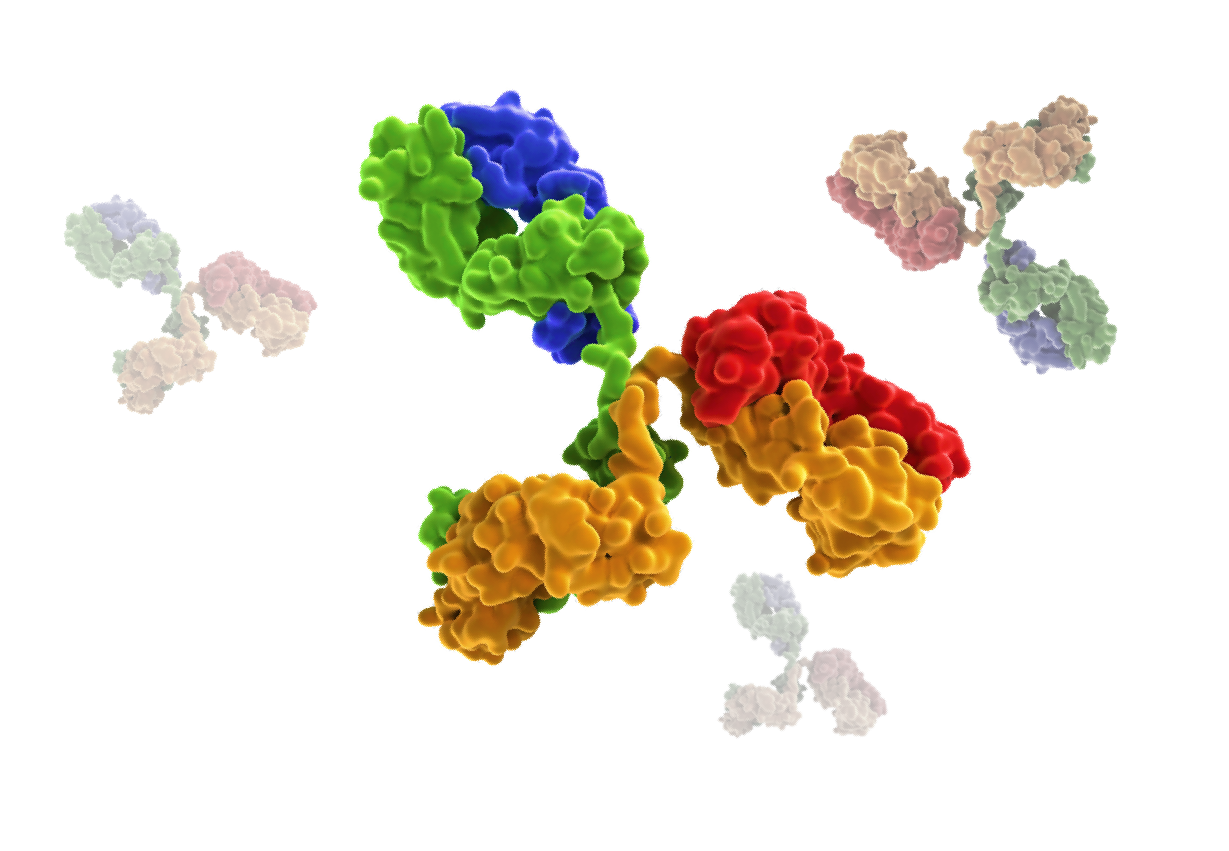
亲和力改造
AI驱动的亲和力(Kd)定量预测模型进行大规模高通量筛选,在更广阔的序列空间中搜索具有合适亲和力的全局最优序列。

可开发性优化
利用多种AI预测模型(聚集性、溶解性和热稳定性等)进行可开发性评估,在高通量筛选中获取性能更加均衡的抗体序列。
免疫原性优化
利用AI精准识别T细胞和B细胞的免疫表位,辅助蛋白的定向改造,确保大分子药物的安全性和有效性。
抗体从头设计
AI驱动的面向特定功能的蛋白分子从头设计,突破自然筛选的序列限制,获得性能更加优异的抗体。

一站式多属性并行优化
AI驱动的亲和力(Kd)定量预测模型进行大规模高通量筛选,在更广阔的序列空间中搜索具有合适亲和力的全局最优序列。

更广阔空间的全局搜索
利用多种AI预测模型(聚集性、溶解性和热稳定性等)进行可开发性评估,在高通量筛选中获取性能更加均衡的抗体序列。

加速抗体研发进程
利用AI精准识别T细胞和B细胞的免疫表位,辅助蛋白的定向改造,确保大分子药物的安全性和有效性。
iNeo–Panorama 系列
- iNeo-Panorama系列产品运用高通量测序技术(NGS)、免疫组化等多种临床“金标准”技术,实现了从DNA、 RNA和蛋白质多个维度的对患者肿瘤细胞中所有蛋白编码基因的检测,是目前比较全面的基因检测方案。
检测内容
新生抗原疫苗的可行性评估
该检测能够整体评估患者是否适合新生抗原疫苗治疗,如新生抗原序列分析、新生抗原免疫原性预测,进而评估患者免疫系统被激活的可能性。 同时检测新生抗原治疗相关标志物,如B2M基因缺陷等,评估新生抗原治疗的潜在疗效。
肿瘤免疫原性评估
检测肿瘤突变负荷(TMB)、肿瘤新生抗原负荷( TNB)以及微卫星稳定状况,进而评估肿瘤免疫原性强弱,提高免疫治疗有效率。
PD-L1表达量的检测
患者肿瘤PD-L1表达量能够预测PD-1/L1抗体疗效,是FDA批准用于预测免疫检查点抑制剂疗效的标志物之一, PD-L1表达量越高,患者越能从PD-1/L1抗体治疗中获益。
疗效相关基因检测
大量的临床试验以及研究表明, 一些基因及其相关通路的表达或突变能够影响对免疫治疗疗效,可以作为分子标志物来指导用药或提示预后。
肿瘤微环境评估
肿瘤微环境中免疫细胞类型及其各自数量代表了肿瘤“冷”“暖”状态,进而能够预测肿瘤免疫治疗疗效以及是否适用新生抗原免疫治疗。
T细胞受体(TCR)检测
肿瘤浸润T细胞是杀伤肿瘤细胞的重要免疫细胞之一,TCR检测能够反映T细胞状态,目前已经作为肿瘤免疫治疗伴随检测,用于预测肿瘤免疫治疗病人的预后。
临床意义
- 国家卫健委之前颁布的《新型抗肿瘤药物临床应用指导原则(2018年版)》,明确指出: 抗肿瘤药物临床应用需在病理组织学确诊后或基因检测后方可使用。广义上讲, 所有肿瘤患者均可以接受基因检测;狭义上讲,根据指南推荐,不同的病种、不同的分期、 出于不同的目的,不同的患者,可选择不同方向的基因检测。 而iNeo–Panorama检测产品,包含所有外显子区域和部分内含子区的突变信息, 以及转录组测序信息,一次采样,满足多种类型检测,让患者无需为需要选择哪些panel检测而烦恼, 同时,使样本最大利用化,满足临床医生的不同专业需求。

产品优势
信息全
深度全外显子测序,包含所有外显子区域和部分内含子区,以及转录组测序,能够满足临床不同分析要求。
范围广
能够匹配全球已上市的抗癌药品,以及Ⅲ期临床研究正在开发的药物。
专有算法三重保障
利用浙江大学、加拿大UBC和iNEO独立自主专利的算法评估,并行评估患者个体化免疫治疗可行性。
专业医学顾问随访
深度全外显子测序,包含所有外显子区域和部分内含子区,以及转录组测序,能够满足临床不同分析要求。
服务流程
Consultation before inspection
Signing informed consent
Sample collection
DNA, RNA sequencing
Report analysis
Professional follow-up
 咨询洽谈
咨询洽谈